Fotobiomodulation, biostimulering, laserterapi – baggrund og grundlæggende principper
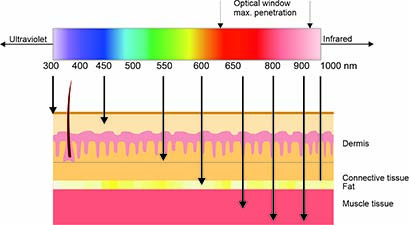
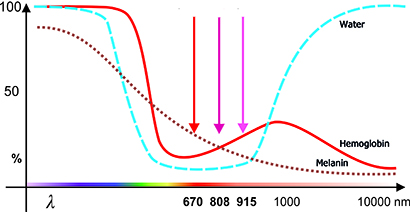
Fotobiomodulationsterapi (PBMT), også kendt som biostimulering eller lavintensitetslaserterapi (LLLT, laserapparater i klasse 3B) og højintensitetslaserterapi (HLLT, laserapparater i klasse 4), er en ikke-invasiv behandlingsmetode. Den anvender lyskilder såsom lasere eller LED'er i det synlige røde (600–700 nm) og nærinfrarøde (700–1100 nm) spektrum. Det skal bemærkes, at bølgelængder over 950 nm har en lav indtrængningsdybde og unødigt opvarmer vævet (på grund af absorption af vand).
I modsætning til kirurgiske lasere ødelægger PBMT ikke væv, men inducerer i stedet fotofysiske og fotokemiske reaktioner på celleniveau. LLLT-laserens effekt er typisk maksimalt 500 mW, mens HLLT kan nå op på flere watt; typiske anvendelser opererer ved ca. 15 W i kontinuerlig bølgetilstand.
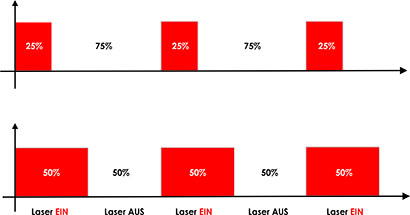
En særlig form for LLLT involverer pulserende lasere som LaserPen eller Physiolaser, der kan opnå spidseffekter på op til 100 W. Pulsbredden (duty cycle, DC) varierer fra ca. 100 til 200 nanosekunder, afhængigt af pulsfrekvensen.
En moderne terapeutisk laser bør ikke kun tilbyde en passende bølgelængde og tilstrækkelig effekt, men også muligheden for modulering og frekvensstyring. Ideelt set er terapeutisk relevante frekvenser forprogrammerede og let tilgængelige.
Tre parametre er særligt afgørende for terapiens succes:
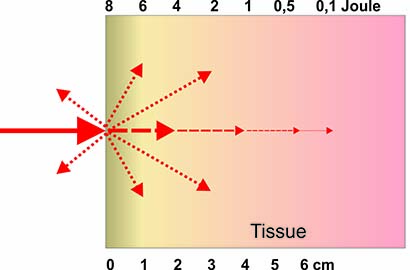
• Den optimale laserbølgelængde, som i høj grad bestemmer lysets indtrængningsdybde (optisk vindue).
• Den passende lasereffekt, som påvirker celleaktiviteten og energiforøgelsen.
• Den korrekte lasermoduleringsfrekvens, som muliggør målrettet stimulering og styring af terapien på informationsniveau.
Biologiske virkninger af laserterapi
Laserstrålen er et skånsomt, men alligevel kraftfuldt terapeutisk redskab. Selv en lavtydelsesslaser på blot 1 mW ved en bølgelængde på 670 nm udsender ca. 3×10¹⁵ fotoner pr. sekund, hvilket illustrerer dens betydelige biologiske potentiale. Dybden af hudpenetrationen afhænger af forskellige faktorer, såsom hudfarve og vævstype.
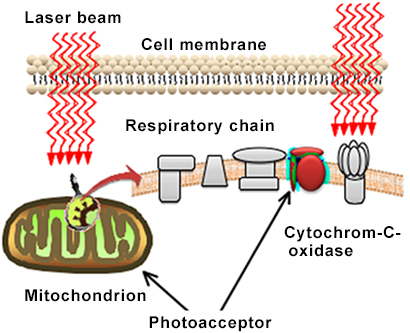
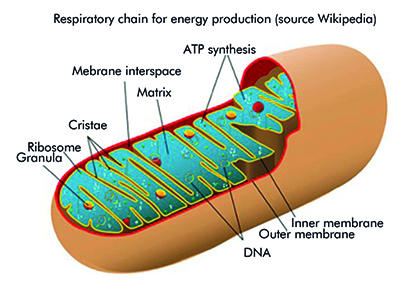
Korrekt anvendelse af laser kan fremkalde en række forskellige reaktioner i levende organismer. Den tilførte laserenergi absorberes af væv og celler, hvilket fører til øget cellulært stofskifte. Denne effekt formidles primært gennem aktivering af mitokondriernes respirationskæde og en efterfølgende stigning i ATP-produktionen.
Ifølge Tina Karu og kolleger betragtes cytochrom c-oxidase som en nøglefotoreceptor, når celler udsættes for monokromatisk rød og nær-infrarød stråling. Der er foreslået flere primære virkningsmekanismer:
Ændringer i redoxegenskaberne hos komponenterne i respirationskæden.
Fotoexcitation af elektronstater, hvilket resulterer i dannelse af singlet-ilt og lokaliseret, kortvarig opvarmning af absorberende kromoforer.
Øget produktion af superoxidanioner, efterfulgt af forhøjede niveauer af hydrogenperoxid (H₂O₂) som et dismutationsprodukt.
Aktivering af en kaskade af intracellulære processer, der involverer ændringer i cellulære homeostaseparametre såsom intracellulært pH (pHi), calciumkoncentration [Ca2+]i[Ca2+]i , cyklisk AMP (cAMP), redoxpotentiale (Eh) og ATP-niveauer. Disse processer tolkes som en del af en fotobiologisk signaltransduktions- og amplifikationsvej (sekundære mekanismer).
Disse mekanismer bidrager samlet til de terapeutiske effekter, der observeres ved fotobiomodulation.
Referencer
Tina Karu, Institut for Laser- og Informationsteknologi, Det Russiske Videnskabsakademi, Troitsk, Moskva-regionen, Den Russiske Føderation
Yderligere relevant arbejde kan findes i publikationerne af:
Herbert Klima, Atomforskningsinstituttet ved de østrigske universiteter, Wien, Østrig
Helmut Walter, Tyskland